Cùng congthuctoanlyhoa khám phá lý thuyết về tính chất hóa học của axit chi tiết và đầy đủ nhất 2023. Tìm hiểu về tính chất hoá học và các loại axit để hiểu rõ hơn về tác động và vai trò quan trọng của chúng trong lĩnh vực hóa học hiện đại.
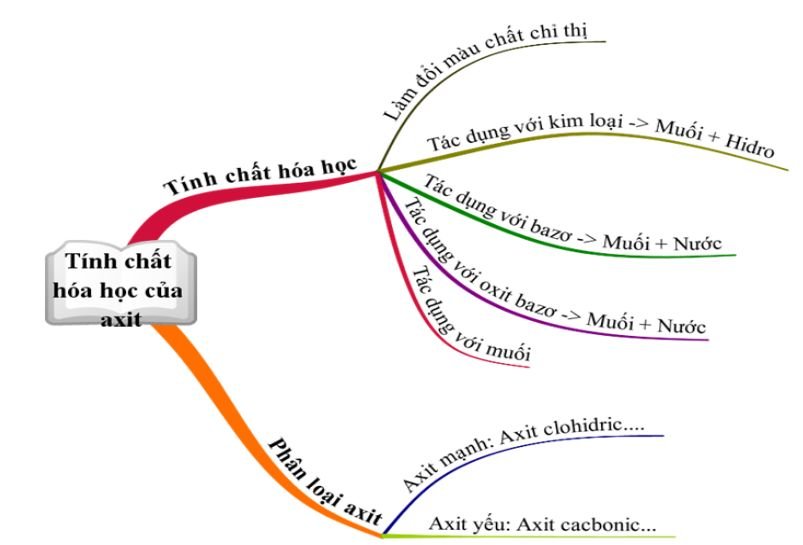
Tính chất hóa học của axit
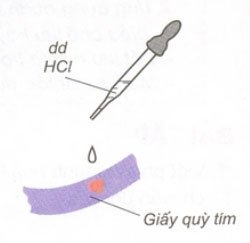
1. Axit làm đổi màu chất chỉ thị
Dung dịch axit làm đổi màu quỳ tím thành đỏ.
Axit tác dụng với kim loại
– Dung dịch axit tác dụng được với một số kim loại tạo thành muối và giải phóng khí hiđro.
– Dãy hoạt động hóa học
, , , , , , , , , , , , , , ,
– Điều kiện: kim loại đứng trước trong dãy hoạt động hóa học của kim loại thì tác dụng với axit.
– Các kim loại Hg, Cu, Ag, Au, Pt …không tác dụng với HCl, H2SO4 loãng.
Ví dụ:
3H2SO4 (dd loãng) + 2Al → Al2(SO4)3 + 3H2
2HCl + Fe → FeCl2 + H2
Chú ý: Axit HNO3 và H2SO4 đặc tác dụng được với nhiều kim loại nhưng không giải phóng hiđro.
Axit tác dụng với bazơ
Axit + bazơ → muối + H2O
Ví dụ:
H2SO4 + Cu(OH)2 → CuSO4 + 2H2O
HCl + NaOH → NaCl + H2O
Phản ứng của axit với bazơ được gọi là phản ứng trung hòa.
Axit tác dụng với oxit bazơ
Axit + oxit bazơ → muối + H2O
Ví dụ:
6HCl + Fe2O3 → FeCl3 + 3H2O
H2SO4 + MgO → MgSO4 + H2O
Ngoài ra, axit còn tác dụng với muối.
Ví dụ:
MgCO3 + 2HCl → MgCl2 + CO2 ↑ + H2O
Na2SO3 + 2HCl → 2NaCl + SO2 ↑ + H2O
Axit mạnh và axit yếu
Dựa vào tính chất hóa học, axit được phân làm 2 loại:
+ Axit mạnh như HCl, H2SO4, HNO3,…
+ Axit yếu như H2S, H2CO3,…