Cùng congthuctoanlyhoa khám phá Lý thuyết Tính chất hóa học của muối chi tiết, đầy đủ nhất 2023. Bài viết cung cấp cho các em cái nhìn sâu sắc về tính chất hoá học của muối, phản ứng trao đổi trong dung dịch, sơ đồ tư duy và cách giải các bài tập Tính chất hóa học của muối. Bài viết này sẽ hỗ trợ cho các em trong việc học tốt môn Hoá học lớp 9.

Tính chất hóa học của muối
1. Tác dụng với kim loại
Dung dịch muối tác dụng với kim loại → muối mới + kim loại mới
– Điều kiện: Kim loại mạnh hơn đẩy kim loại yếu hơn ra khỏi muối
Ví dụ:
Fe + CuSO4 → FeSO4 + Cu↓
Cu + 2AgNO3 → Cu(NO3)2 + 2Ag↓
2. Tác dụng với axit
Dung dịch muối tác dụng với axit → muối mới + axit mới
– Điều kiện : sản phẩm tạo thành phải có chất khí hoặc chất kết tủa hoặc nước
Ví dụ:
AgNO3 + HCl → AgCl ↓ + HNO3
CaCO3 + 2HCl → CaCl2 + CO2↑ + H2O
3. Tác dụng với dung dịch muối
Dung dịch muối tác dụng với dung dịch muối → 2 muối mới
– Điều kiện: sản phẩm tạo thành phải có chất khí hoặc chất kết tủa hoặc nước
Ví dụ:
AgNO3 + NaCl → NaNO3 + AgCl↓
BaCl2 + K2SO4 → 2KCl + BaSO4 ↓
4. Tác dụng với dung dịch bazơ
Dung dịch muối tác dụng với dung dịch bazơ → muối mới + bazơ mới
– Điều kiện: sản phẩm tạo thành phải có chất khí hoặc chất kết tủa hoặc nước
Ví dụ:
K2CO3 + Ba(OH)2 → 2KOH + BaCO3↓
CuCl2 + 2NaOH → Cu(OH)2 ↓ + 2NaCl
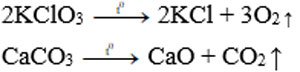
5. Phản ứng phân hủy muối
– Nhiều muối bị phân hủy ở nhiệt độ cao như: KClO3, KMnO4, CaCO3,…
Phản ứng trao đổi trong dung dịch
1. Định nghĩa:
Phản ứng trao đổi là phản ứng hóa học, trong đó hai hợp chất tham gia phản ứng trao đổi với nhau những thành phần cấu tạo của chúng để tạo ra những hợp chất mới.
2. Điều kiện xảy ra phản ứng trao đổi
Phản ứng trao đổi trong dung dịch của các chất chỉ xảy ra nếu sản phẩm tạo thành có chất không tan hoặc chất khí.
Ví dụ:
CuSO4 + 2NaOH → Na2SO4 + Cu(OH)2↓
K2SO4 + NaOH: Phản ứng không xảy ra.
– Chú thích: phản ứng trung hòa cũng thuộc loại phản ứng trao đổi và luôn xảy ra.
HCl + NaOH → NaCl + H2O
Sơ đồ tư duy: Tính chất hóa học của muối
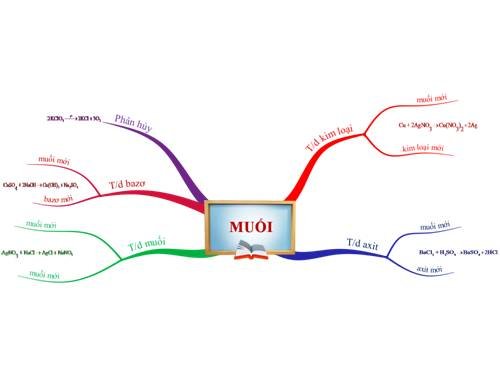
Giải bài tập Tính chất hóa học của muối
Bài 1 trang 33 sgk Hóa 9
Hãy dẫn ra một dung dịch muối khi tác dụng với một dung dịch chất khác thì tạo ra:
a) Chất khí;
b) Chất kết tủa.
Viết phương trình hóa học.
Đáp án hướng dẫn giải chi tiết
a) Ta chọn các muối cacbonat hoặc muối sunfit tác dụng với axit mạnh.
Thí dụ: CaCO3 + HCl → CaCl2 + CO2↑ + H2O
Na2SO3 + H2SO4 → Na2SO4 + SO2↑ + H2O
Na2CO3 + 2HCl → 2NaCl + CO2 + H2O
NaHCO3 + HCl → NaCl + H2O + CO2
b) Ta dựa vào bảng tính tan của muối để chọn các muối không tan (BaSO4, AgCl, BaCO3…) hoặc bazơ không tan, từ đó tìm ra muối và chất tham gia phản ứng còn lại, thí dụ:
BaCl2 + H2SO4 → 2HCl + BaSO4↓
Na2CO3 + Ba(NO3)2 → 2NaNO3 + BaCO3↓
CuSO4 + 2NaOH → Cu(OH)2 + Na2SO4↓
NaCl + AgNO3 → NaNO3 + AgCl
Bài 2 trang 33 sgk Hóa 9
Có 3 lọ không nhãn, mỗi lọ đựng một dung dịch muối: CuSO4, AgNO3, NaCl. Hãy dùng những dung dịch có sẵn trong phòng thí nghiệm để nhận biết chất đựng trong mỗi lọ. Viết các phương trình hóa học.
Đáp án hướng dẫn giải chi tiết
Dùng dung dịch NaCl tự pha chế để nhận biết dung dịch AgNO3
Xuất hiện chất kết tủa trắng AgCl
AgNO3 + NaCl → AgCl ↓ + NaNO3
Dùng dung dịch NaOH trong phòng thí nghiệm để nhận biết dung dịch CuSO4 màu xanh lam
CuSO4 + NaOH → Cu(OH)2 + Na2SO4
Dung dịch còn lại trong lọ không nhãn là dung dịch NaCl.
Bài 3 trang 33 sgk Hóa 9
Có những dung dịch muối sau: Mg(NO3)2, CuCl2. Hãy cho biết muối nào có thể tác dụng với:
a) Dung dịch NaOH;
b) Dung dịch HCl;
c) Dung dịch AgNO3.
Nếu có phản ứng, hãy viết các phương trình hóa học.
Đáp án hướng dẫn giải chi tiết
a) Cả hai muối tác dụng với dung dịch NaOH vì sản phẩm tạo thành có Mg(OH)2, Cu(OH)2 không tan,
Mg(NO3)2 + 2NaOH → 2NaNO3 + Mg(OH)2↓
CuCl2 + 2NaOH → 2NaCl + Cu(OH)2↓
b) Không có muối nào tác dụng với dung dịch HCl vì không có chất kết tủa hay chất khí tạo thành.
c) Chỉ có muối CuCl2 tác dụng với dung dịch AgNO3 vì sản phẩm tạo thành có AgCl không tan.
CuCl2 + 2AgNO3 → 2AgCl↓ + Cu(NO3)2
Vậy là các em đã tìm hiểu xong bài học về Lý thuyết Tính chất hóa học của muối. Mong các em sẽ học ngày càng tốt hơn nữa môn Hoá học 9.